|
Analyse
des forces mises en jeu dans une bouteille de
fluide frigorigène :
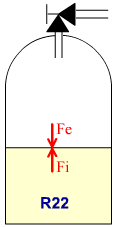 |
Dans une bouteille de R22,
la surface du fluide frigorigène
est soumise à l'action de deux
forces :
Fe = force externe exercée par
la vapeur de fluide frigorigène
sur la surface du liquide.
Fi = force interne exercée par
le liquide sur sa surface.
Naturellement, le fluide
frigorigène établit un équilibre
entre ses 2 forces. C'est à dire
qu'il essaie de maintientir Fe=Fi.
La bouteille étant
fermée, la quantité de vapeurs
contenue dans celle-ci engendre une force
Fe qui compense celle interne au liquide...
Rien ne se passe dans la bouteille.
|
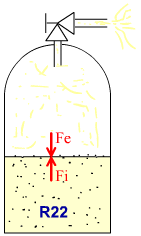 |
En ouvrant la vanne de la
bouteille, des vapeurs s'échappent.
La pression exercée par ces vapeurs
sur la surface du liquide diminue. La
force Fe qu'elles engendrent diminue aussi.
Elle devient alors inférieure à
Fi. Le fluide frigorigène se met
à bouillir afin de fournir des
vapeurs pour rétablir l'équilibre
naturel. Malheureusement, comme les vapeurs
s'échappent de la bouteille, l'ébulition
du liquide ne permet pas de rétablir
l'équilibre...
Ainsi, nous pouvons conclure
que le fluide frigorigène bout
si Fe devient inférieur à
Fi.
|
Relation
pression-température :
 |
Un mélange liquide-gaz
de R134a à 20°C a une pression
de 4,7 bar.
C'est la relation pression-température
pour le mélange liquide-gaz de
R134a.
Chaque fluide possède sa propre
relation pression-température.
Ainsi, un mélange liquide-gaz de
R22 à 20°C aura une pression
de 8,1bar qui est différente de
celle du mélange liquide-gaz de
R134a.
Connaissant la température
d'un mélange liquide-gaz d'un fluide,
on peut connaître sa pression et
vis-versa.
C'est pourquoi sur les manomètres
utilisés par les frigoristes, il
y a une échelle de pression et
des échelles de température
pour des fluides donnés.
Il est aussi possible de faire la correspondance
pression-température pour un mélange
liquide-gaz à l'aide d'une réglette
de conversion.

Réglette
de conversion offerte par Calorie
|
 |
Si la température
augmente de 10°C, l'agitation moléculaire
va augmenter dans le liquide. La force
interne Fi deviendra supérieure
à la force externe Fe. Le fluide
frigorigène va donc essayer de
rétablir l'équilibre entre
son liquide et sa vapeur. Pour cela, une
faible quantité de liquide va s'évaporer
pour fournir des vapeurs. Cette quantité
de vapeurs supplémentaire permet
à Fe de croître aussi, et
dans la même proportion de Fi. Grâce
à l'évaporation de la faible
quantité de liquide, le fluide
frigorigène a réussit à
rétablir l'équilibre entre
la force exercée par sa vapeur
et celle exercée par son liquide.
On retrouve alors Fe=Fi.
Comme on retrouve plus de vapeurs, la
pression augmente... 6,6 bar, c'est la
pression d'un mélange liquide-gaz
de R134a à 30°C.
|
 |
Il suffit d'une goutte de
liquide pour que la relation pression-température
soit applicable. Ici la condition est
réalisée. Nous pouvons donc
dire : 6,6 bar, c'est la pression d'un
mélange liquide-gaz de R134a à
30°C.
|
Vapeurs
surchaufées :
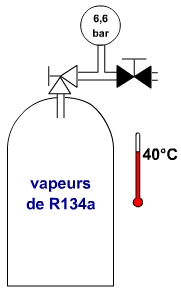 |
Si nous plaçons la
bouteille précédente dans
une ambiance à + 40°C. L'agitation
moléculaire augmente dans la goutte
de liquide qui s'évapore. Malheureusement,
elle ne fournit plus suffisamment de vapeurs
pour faire augmenter la pression. Celle-ci
reste égale à 6,6 bar. La
force exercée par la pression de
vapeur Fe ne peut donc plus augmenter.
L'élévation de la température
ambiante à 40°C à fait
évaporer tout le liquide. Il n'y
a donc plus relation pression-température.
6,6 bar était la pression d'un
mélange liquide-gaz de R134a à
30°C. Ici nous avons des vapeurs à
40°C.
Elles sont donc surchauffées de
40°C - 30°C= 10°C.
|
|
